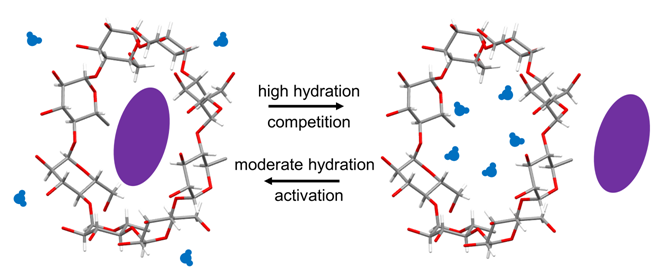
Конкурирующая роль воды при инкапсуляции индометацина и летучих «гостей» нативными циклодекстринами
DOI: 10.6060/mhc224319g
Аннотация
Гидратация снижает эффективность инкапсуляции лекарственных средств нативными циклодекстринами при добавлении воды выше определенного порогового уровня. В насыщенных гидратах γ-циклодекстрина и β-циклодекстрина гидратная вода конкурирует с индометацином при твердофазном включении в полость этих «хозяев». Подобный эффект гидратации в случае включения индометацина коррелирует с влиянием гидратной воды на включение летучих органических «гостей» нативными циклодекстринами. Для этих гостей конкурирующий эффект гидратации γ-циклодекстрина оценивался также по изотермам сорбции паров и оказался выше, чем у β-циклодекстрина, но в большинстве случаев ниже, чем у α-циклодекстрина. В работе было определено сродство сухого γ-циклодекстрина к воде и органическим гостям, и наблюдался значительный эффект исключения по размеру «гостя», который способствует конкуренции «вода-гость». Соотношение конкурирующей и активирующей роли воды для трех исследованных нативных циклодекстринов коррелирует с параметрами их элементарных ячеек в гидратах и в высушенном состоянии.
Литература
References
Spyrakis F., Ahmed M.H., Bayden A.S., Cozzini P., Mozzarelli A., Kellogg G.E. J. Med. Chem. 2017, 60, 6781–6828. https://doi.org/10.1021/acs.jmedchem.7b00057
Gorbatchuk V.V., Ziganshin, M.A., Solomonov B.N. Biophys. Chem. 1999, 81, 107–123. https://doi.org/10.1016/S0301-4622(99)00087-3
Mironov N.A., Breus V.V., Gorbatchuk V.V., Solomonov B.N., Haertlé T. J. Agric. Food Chem. 2003, 51, 2665–2673. https://doi.org/10.1021/jf020896m
Gorbatchuk V.V., Mironov N.A., Solomonov B.N., Habicher W.D. Biomacromolecules 2004, 5, 1615–1623. https://doi.org/10.1021/bm049743t
Gatiatulin A.K., Osel’skaya V.Y., Ziganshin M.A., Gorbatchuk V.V. RSC Adv. 2019, 9, 37778–37787. https://doi.org/10.1039/C9RA08710A
Gorbatchuk V.V., Gatiatulin A.K., Ziganshin M.A., Gubaidullin A.T., Yakimova L.S. J. Phys. Chem. B 2013, 117, 14544–14556. https://doi.org/10.1021/jp408059b
Jambhekar S.S., Breen P. Drug Discov. Today 2016, 21, 363–368. https://doi.org/10.1016/j.drudis.2015.11.016
Loftsson T., Brewster M.E. J. Pharm. Pharmacol. 2010, 62, 1607–1621. https://doi.org/10.1111/j.2042-7158.2010.01030.x
Couillaud B.M., Espeau P., Mignet N., Corvis Y. ChemMedChem 2019, 14, 8–23. https://doi.org/10.1002/cmdc.201800612
Del Valle E.M.M. Process Biochem. 2004, 39, 1033–1046. https://doi.org/10.1016/S0032-9592(03)00258-9
Salústio P.J., Feio G., Figueirinhas J.L., Pinto J.F., Cabral Marques H. M. Eur. J. Pharm. Biopharm. 2009, 71, 377–386. https://doi.org/10.1016/j.ejpb.2008.09.027
Pereva S., Sarafska T., Bogdanova S., Spassov T. J. Drug Deliv. Sci. Technol. 2016, 35, 34–39. https://doi.org/10.1016/j.jddst.2016.04.006
Adhage N.A., Vavia P.R. Pharm. Pharmacol. Commun. 2000, 6, 13–17. https://doi.org/10.1211/146080800128735412
Wei W., Evseenko V.I., Khvostov M.V., Borisov S.A., Tolstikova T.G., Polyakov N.E., Dushkin A.V., Xu W., Min L., Su W. Molecules 2021, 26, 1513. https://doi.org/10.3390/molecules26061513
Rinaldi L., Binello A., Stolle A., Curini M., Cravotto G. Steroids 2015, 98, 58–62. https://doi.org/10.1016/j.steroids.2015.02.016
Nozawa Y., Morioka Y., Sadzuka Y., Miyagishima A., Hirota S., Guillory J.K. Pharm. Acta Helv. 1997, 72, 113–117. https://doi.org/10.1016/S0031-6865(97)00003-4
Brusnikina M., Silyukov O., Chislov M., Volkova T., Proshin, A., Terekhova I. J. Therm. Anal. Calorim. 2017, 127, 1815–1824. https://doi.org/10.1007/s10973-016-5955-z
Mura P., Faucci M. T., Parrini P. L., Furlanetto S., Pinzauti S. Int. J. Pharm. 1999, 179, 117–128. https://doi.org/10.1016/S0378-5173(98)00390-1
Gatiatulin A.K., Ziganshin M.A., Gorbatchuk V. V. Front. Chem. 2020, 7, 1–8. https://doi.org/10.3389/fchem.2019.00933
Gatiatulin A.K., Osel’skaya V.Y., Ziganshin M.A., Gorbatchuk V.V. Phys. Chem. Chem. Phys. 2018, 20, 26105–26116. https://doi.org/10.1039/C8CP03104E
Yoshii H., Furuta T., Yasunishi A., Hirano H. J. Biochem. 1994, 115, 1035–1037. https://doi.org/10.1093/oxfordjournals.jbchem.a124452
Gorbatchuk V.V., Tsifarkin A.G., Antipin I.S., Solomonov B.N., Konovalov A.I., Lhotak P., Stibor I. J. Phys. Chem. B 2002, 106, 5845–5851. https://doi.org/10.1021/jp014352j
Gatiatulin A.K., Ziganshin M.A., Yumaeva G.F., Gubaidullin A.T., Suwińska K., Gorbatchuk V.V. RSC Adv. 2016, 6, 61984–61995. https://doi.org/10.1039/C6RA11378H
Lan P.T., Minh V.X., Khoa L.H., Kabirov D.N., Ngoan N.T., Usacheva T.R. Russ. J. Phys. Chem. A 2021, 95, 887–893. https://doi.org/10.1134/S0036024421050113
Kashapov R.R., Lykova A.A., Mamedova V.L., Kadyrova S.F., Sapunova A.S., Voloshina A.D., Mamedov V.A., Zakharova L.Y. J. Drug Deliv. Sci. Technol. 2020, 59, 101857. https://doi.org/10.1016/j.jddst.2020.101857
O’Brien M., McCauley J., Cohen E. Analytical Profiles of Drug Substances 1984, 13, 211–238. https://doi.org/10.1016/S0099-5428(08)60192-6
Surwase S.A., Boetker J.P., Saville D., Boyd B.J., Gordon K.C., Peltonen L., Strachan C.J. Mol. Pharm. 2013, 10, 4472–4480. https://doi.org/10.1021/mp400299a
Crowley K.J., Zografi G. J. Pharm. Sci. 2002, 91, 492–507. https://doi.org/10.1002/jps.10028
Armarego W.L.F., Chai C.L.L. Purification of Laboratory Chemicals. Burlington: Butterworth-Heinemann, 2009. 760 p.
Greenspan L. J. Res. Natl. Bur. Stand. Sect. A Phys. Chem. 1977, 81A, 89. https://doi.org/10.6028/jres.081A.011
Gorbatchuk V.V., Tsifarkin A.G., Antipin I.S., Solomonov B.N., Konovalov A.I., Seidel J., Baitalov F. J. Chem. Soc. Perkin Trans. 2 2000, 11, 2287–2294. https://doi.org/10.1039/b003477k
Yakimova L.S., Ziganshin M.A., Sidorov V.A., Kovalev V.V., Shokova E.A., Tafeenko V.A., Gorbatchuk V.V. J. Phys. Chem. B 2008, 112, 15569–15575. https://doi.org/10.1021/jp804277u
Gorbatchuk V.V., Antipin I.S., Tsifarkin A.G., Solomonov B.N., Konovalov A.I. Mendeleev Commun. 1997, 7, 215–217. https://doi.org/10.1070/MC1997v007n06ABEH000807
Abundo M., Accardi L., Finazzi Agrò A., Mei G., Rosato N. Biophys. Chem. 1996, 58, 313–323. https://doi.org/10.1016/0301-4622(95)00111-5
Gorbatchuk V.V., Tsifarkin A.G., Antipin I.S., Solomonov B.N., Konovalov A.I. Mendeleev Commun. 1999, 9, 11–13. https://doi.org/10.1070/MC1999v009n01ABEH000989
Zelenina L.N., Chusova T.P., Isakov A.V., Rodionova T.V., Villevald G.V., Manakov A.Y. J. Chem. Thermodyn. 2021, 158, 106424. https://doi.org/10.1016/j.jct.2021.106424
Nakai Y., Yamamoto K., Terada K., Kajiyama A., Sasaki I. Chem. Pharm. Bull. 1986, 34, 2178–2182. https://doi.org/10.1248/cpb.34.2178
Hădărugă N.G., Bandur G.N., David I., Hădărugă D.I. Environ. Chem. Lett. 2019, 17, 349–373. https://doi.org/10.1007/s10311-018-0806-8
Manor P.C., Saenger W. J. Am. Chem. Soc. 1974, 96, 3630–3639. https://doi.org/10.1021/ja00818a042
Steiner T., Koellner G. J. Am. Chem. Soc. 1994, 116, 5122–5128. https://doi.org/10.1021/ja00091a014
Hingerty B.E., Betzel C., Saenger W. American Crystallographic Association, Series 2 1984, 12, 37.
Harata K. Bull. Chem. Soc. Jpn. 1987, 60, 2763–2767. https://doi.org/10.1246/bcsj.60.2763
Marcolli C. Atmos. Chem. Phys. 2020, 20, 3209–3230. https://doi.org/10.5194/acp-20-3209-2020
Gatiatulin A.K., Osel’skaya V.Y., Ziganshin M.A., Gorbatchuk V.V. J. Therm. Anal. Calorim. 2021, 146, 2417–2422. https://doi.org/10.1007/s10973-020-10428-0
Legendre B., Feutelais Y. J. Therm. Anal. Calorim. 2004, 76, 255–264. https://doi.org/10.1023/B:JTAN.0000027824.55280.37
Nakai Y., Yamamoto K., Terada K., Sasaki I. Yakugaku Zasshi 1986, 106, 420–424. https://doi.org/10.1248/yakushi1947.106.5_420
Frieler L., Ho T.M., Anthony A., Hidefumi Y., Yago A.J.E., Bhandari B.R. J. Food Sci. Technol. 2019, 56, 1519–1529. https://doi.org/10.1007/s13197-019-03643-7
Andronis V., Yoshioka M., Zografi G. J. Pharm. Sci. 1997, 86, 346–351. https://doi.org/10.1021/js9602711
Andronis V., Zografi G. J. Non. Cryst. Solids 2000, 271, 236–248. https://doi.org/10.1016/S0022-3093(00)00107-1