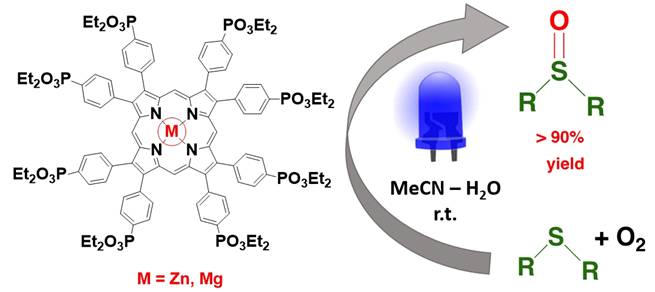
Mg and Zn Complexes with Phosphonate Substituted β-Octaphenylporphyrin as Photocatalysts for Oxidation of Sulfides
Аннотация
2,3,7,8,12,13,17,18-Окта[(4-диэтоксифосфорил)фенил]порфиринат магния (MgOPPP) был получен с хорошим выходом в реакции свободного основания порфирина с ацетатом магния в ДМФА при 130°С. Полученный комплекс использовали как катализатор для селективного фотоокисления сульфидов в сульфоксиды кислородом. Как диалкил-, так и алкиларилсульфиды дали сульфоксиды с выходами близкими к количественным при проведении реакции при облучении синим светодиодом (30 Вт) в смеси ацетонитрил/вода (5:1, об./об.) при использовании 0.05 мол.% MgOPPP в качестве фотокатализатора. Сравнительные исследования показали, что порфиринат цинка ZnOPPP позволяет сократить время проведения реакции без потери её селективности.
Литература
Shalan H., Colbert A., Nguyen T.T., Kato M., Cheruzel L. Inorg. Chem. 2017, 56, 6558–6564. https://doi.org/10.1021/acs.inorgchem.7b00685
Morozkov G.V., Abel A.S., Filatov M.A., Nefedov S.E., Roznyatovsky V.A., Cheprakov A.V., Mitrofanov A.Y., Ziankou I.S., Averin A.D., Beletskaya I.P., Michalak J., Bucher C., Bonneviot L., Bessmertnykh-Lemeune A. Dalton Trans. 2022, 51, 13612–13630. https://doi.org/10.1039/D2DT01364A
DiLuzio S., Connell T.U., Mdluli V., Kowalewski J.F., Bernhard S. J. Am. Chem. Soc. 2022, 144, 1431–1444. https://doi.org/10.1021/jacs.1c12059
Mahmood Z., He J., Cai S., Yuan Z., Liang H., Chen Q., Huo Y., König B., Ji S. Chem. Eur. J. 2023, 29, e202202677. https://doi.org/10.1002/chem.202202677
Costa E Silva R., Oliveira da Silva L., de Andrade Bartolomeu A., Brocksom T.J., de Oliveira K.T. Beilstein J. Org. Chem. 2020, 16, 917–955. https://doi.org/10.3762/bjoc.16.83
Harvey P.D. J. Mater. Chem. C 2021, 9, 16885–16910. https://doi.org/10.1039/D1TC04147A
Rybicka-Jasińska K., Wdowik T., Łuczak K., Wierzba A.J., Drapała O., Gryko D. ACS Org. Inorg. Au 2022, 2, 422–426. https://doi.org/10.1021/acsorginorgau.2c00025
Mansuy D. C. R. Chim. 2007, 10, 392–413. https://doi.org/10.1016/j.crci.2006.11.001
Pereira M.M., Dias L.D., Calvete M.J.F. ACS Catalysis 2018, 8, 10784–10808. https://doi.org/10.1021/acscatal.8b01871
Chaubey S., Singh P., Singh C., Singh S., Shreya S., Yadav R.K., Mishra S., Jeong, Y.-j., Biswas, B. K., Kim, T. W. J. CO2 Util. 2022, 59, 101968. https://doi.org/10.1016/j.jcou.2022.101968
Ezzayani K., Khelifa A.B., Guesmi A., Hamadi N.B., El-Fattah W.A., Nasri H. J. Mol. Struct. 2022, 1258, 132663. https://doi.org/10.1016/j.molstruc.2022.132663
Borah K.D., Bhuyan J. Dalton Trans. 2017, 46, 6497–6509. https://doi.org/10.1039/C7DT00823F
Hanusa T.P., Group 1 and 2 Metals. In Reference Module in Chemistry, Molecular Sciences and Chemical Engineering, Elsevier: 2014.
Takeda J., Ohya T., Sato M. Chem. Pharm. Bull. 1990, 38, 264–266. https://doi.org/10.1248/cpb.38.264
Shukaev A.V., Ermakova E.V., Fang Y., Kadish K.M., Nefedov S.E., Tafeenko V.A., Michalak J., Bessmertnykh-Lemeune A. Inorg. Chem. 2023, 62, 3431–3444. https://doi.org/10.1021/acs.inorgchem.2c03466
Lindsey J.S., Woodford J.N. Inorg. Chem. 1995, 34, 1063–1069. https://doi.org/10.1021/ic00109a011
Miller S. Environ. Sci. Technol. 1990, 24, 1286–1289. https://doi.org/10.1021/es00079a600
Stingl K.A., Tsogoeva S.B. Tetrahedron: Asymm. 2010, 21, 1055–1074. https://doi.org/10.1016/j.tetasy.2010.05.020
Liu Y., Howarth A.J., Hupp J.T., Farha O.K. Angew. Chem., Int. Ed. 2015, 54, 9001–9005. https://doi.org/10.1002/ange.201503741
Laudadio G., Straathof N.J.W., Lanting M.D., Knoops B., Hessel V., Noël T. Green Chem. 2017, 19, 4061–4066. https://doi.org/10.1039/C7GC01973D
Matavos-Aramyan S., Soukhakian S., Jazebizadeh M.H. Phosphorus Sulfur Silicon Relat. Elem. 2020, 195, 181–193. https://doi.org/10.1080/10426507.2019.1672691
Baciocchi E., Rol C., Scamosci E., Sebastiani G.V. J. Org. Chem. 1991, 56, 5498–5502. https://doi.org/10.1021/jo00019a005
Baciocchi E., Crescenzi C., Lanzalunga O. Tetrahedron 1997, 53, 4469–4478. https://doi.org/10.1016/S0040-4020(97)00119-1
Baciocchi E., Del Giacco T., Gerini M.F., Lanzalunga O. Org. Lett. 2006, 8, 641–644. https://doi.org/10.1021/ol052834y
Zhou X.-T., Ji H.-B. Catal. Commun. 2014, 53, 29–32. https://doi.org/10.1016/j.catcom.2014.04.021
Chen L., Yang Y., Jiang D. J. Am. Chem. Soc. 2010, 132, 9138–9143. https://doi.org/10.1021/ja1028556
To W.-P., Liu Y., Lau T.-C., Che C.-M. Chem. Eur. J. 2013, 19, 5654–5664. https://doi.org/10.1002/chem.201203774
Mojarrad A.G., Zakavi S. Catal. Sci. Technol. 2018, 8, 768–781. https://doi.org/10.1039/C7CY02308A
Pereira C.F., Figueira F., Mendes R.F., Rocha J., Hupp J.T., Farha O.K., Simões M.M.Q., Tomé J.P.C., Paz F.A.A. Inorg. Chem. 2018, 57, 3855–3864. https://doi.org/10.1021/acs.inorgchem.7b03214
Jiang J., Luo R., Zhou X., Chen Y., Ji H. Adv. Synth. Catal. 2018, 360, 4402–4411. https://doi.org/10.1002/adsc.201800730
Abdulaeva I.A., Birin K.P., Chassagnon R., Bessmertnykh-Lemeune A. Catalysts 2023, 13, 402. https://doi.org/10.3390/catal13020402
Fujita S., Sato H., Kakegawa N., Yamagishi A. J. Phys. Chem. B 2006, 110, 2533–2540. https://doi.org/10.1021/jp055254r
Clennan E.L. Acc. Chem. Res. 2001, 34, 875–884. https://doi.org/10.1021/ar0100879
Bonesi S.M., Fagnoni M., Monti S., Albini A. Tetrahedron 2006, 62, 10716–10723. https://doi.org/10.1016/j.tet.2006.07.110
Bonesi S.M., Carbonell E., Garcia H., Fagnoni M., Albini A. Appl. Catal., B 2008, 79, 368–375. https://doi.org/10.1016/j.apcatb.2007.10.037
Demas J.N., Harris E.W., McBride R.P. J. Am. Chem. Soc. 1977, 99, 3547–3551. https://doi.org/10.1021/ja00453a001
Anderson C.P., Salmon D.J., Meyer T.J., Young R.C. J. Am. Chem. Soc. 1977, 99, 1980–1982. https://doi.org/10.1021/ja00448a054
Hikita T., Tamaru K., Yamagishi A., Iwamoto T. Inorg. Chem. 1989, 28, 2221–2223. https://doi.org/10.1021/ic00310a043
Rajkumar E., Rajagopal S. Photochem. Photobiol. Sci. 2008, 7, 1407–1414. https://doi.org/10.1039/b806974c
Neveselý T., Svobodová E., Chudoba J., Sikorski M., Cibulka R. Adv. Synth. Catal. 2016, 358, 1654–1663. https://doi.org/10.1002/adsc.201501123
Gu C.-L., Foote C.S., Kacher M.L. J. Am. Chem. Soc. 1981, 103, 5949–5951. https://doi.org/10.1021/ja00409a073
Kamata K., Hirano T., Mizuno N. Chem. Commun. 2009, 3958–3960. https://doi.org/10.1039/B907952A
Hosseini-Eshbala F., Sedrpoushan A., Dehdashti M.N., Breit B., Mohanazadeh F., Veisi H. Mater. Sci. Eng. C 2019, 103, 109814. https://doi.org/10.1016/j.msec.2019.109814