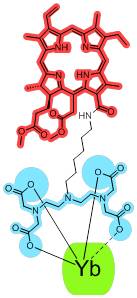
Иттербиевые комплексы производных хлорина е6 для таргетной NIR-II биовизуализации
Аннотация
Получены два новых производных хлорина е6, содержащих хелатирующие группы на периферии макроцикла, а также были синтезированы и охарактеризованы их комплексы с иттербием. Обнаружено, что излучение иона иттербия в ближней инфракрасной области II (NIR-II) сенсибилизировалось хлоринами, при этом эффективность сенсибилизации зависела от расстояния между атомом Yb и хлориновым ядром. Проведены детальные исследования люминесценции комплексов иттербия и эксперименты in vitro, в ходе которых изучена кинетика накопления в опухолевых клетках. Благодаря своим свойствам полученные металлокомплексы могут найти потенциальное применение в флуоресцентной визуализации в NIR-II диапазоне.
Литература
Glunde K., Jacobs M.A., Pathak A.P., Artemov D., Bhujwalla Z.M. NMR Biomed. 2009, 22, 92-103. https://doi.org/10.1002/nbm.1269
Bünzli J.C.G. Chem. Lett. 2009, 38, 104-109. https://doi.org/10.1246/cl.2009.104
Bünzli J.C.G. Chem. Rev. 2010, 110, 2729-2755. https://doi.org/10.1021/cr900362e
Fang H., Chen Y., Jiang Z., He W., Guo Z. Acc. Chem. Res. 2023, 56, 258-269. https://doi.org/10.1021/acs.accounts.2c00643
Wang R., Zhang F. J. Mater. Chem. B 2014, 2, 2422-2443. https://doi.org/10.1039/c3tb21447h
Weissleder R. Nat. Biotechnol. 2001, 19, 316-317. https://doi.org/10.1038/86684
Konig K. J. Microsc. 2000, 200, 83-104. https://doi.org/10.1046/j.1365-2818.2000.00738.x
Ning Y., Chen S., Chen H., Wang J.X., He S., Liu Y.W., Cheng Z., Zhang J.L. Inorg. Chem. Front. 2019, 6, 1962-1967. https://doi.org/10.1039/C9QI00157C
Ning Y., Tang J., Liu Y.W., Jing J., Sun Y., Zhang J.L. Chem. Sci. 2018, 9, 3742-3753. https://doi.org/10.1039/C8SC00259B
Kovalenko A.D., Pavlov A.A., Ustinovich I.D., Kalyakina A.S., Goloveshkin A.S., Marciniak Ł., Lepnev L.S., Burlov A.S., Schepers U., Bräse S., Utochnikova V.V. Dalton Trans. 2021, 50, 3786-3791. https://doi.org/10.1039/D0DT03913F
Get'man E.I., Oleksii Y.A., Radio S.V., Ardanova L.I. Fine Chemical Technologies 2020, 15, 54-62. https://doi.org/10.32362/2410-6593-2020-15-5-54-62
D'Aléo A., Bourdolle A., Brustlein S., Fauquier T., Grichine A., Duperray A., Baldeck P.L., Andraud C., Brasselet S., Maury O. Angew. Chemie 2012, 124, 6726-6729. https://doi.org/10.1002/ange.201202212
Khan Y., Han D., Pierre A., Ting J., Wang X., Lochner C.M., Bovo G., Yaacobi-Gross N., Newsome C., Wilson R., Arias A.C. Proc. Natl. Acad. Sci. U. S. A. 2018, 115, E11015-E11024. https://doi.org/10.1073/pnas.1813053115
He M., Ye M., Li B., Wu T., Lu C., Liu P., Li H., Zhou X., Wang, Y., Liang, T., Li H., Li Ch. Sens. Actuators, B 2022, 364, 131868. https://doi.org/10.1016/j.snb.2022.131868
Yan Y., Li S., Zhang Z.H., Qu J., Wang J.Y. Spectrochim. Acta, Part A 2021, 260, 119988. https://doi.org/10.1016/j.saa.2021.119988
Bünzli J.-C.G., Eliseeva S.V. Basics of Lanthanide Photophysics. In: Lanthanide Luminescence. Springer Series on Fluorescence, Vol. 7 (Hänninen P., Härmä H., Eds.), Springer, Berlin, Heidelberg, 2010. pp. 1-45. https://doi.org/10.1007/4243_2010_3
Bünzli J.-C.G. Coord. Chem. Rev. 2015, 293-294, 19-47. https://doi.org/10.1016/j.ccr.2014.10.013
Sy M. Chem. Commun. 2016, 52, 5080–5095. https://doi.org/10.1039/C6CC00922K
Berezin M.Y., Achilefu S. Chem. Rev. 2010, 110, 2641-2684. https://doi.org/10.1021/cr900343z
Wu F., Yue L., Yang L., Wang K., Liu G., Luo X., Zhu X. Colloids Surf., B 2019, 175, 272-280. https://doi.org/10.1016/j.colsurfb.2018.11.054
Dasari S., Singh S., Kumar P., Sivakumar S., Patra A.K. Eur. J. Med. Chem. 2019, 163, 546-559. https://doi.org/10.1016/j.ejmech.2018.12.010
Cable M.L., Levine D.J., Kirby J.P., Gray H.B., Ponce A. Adv. Inorg. Chem. 2011, 63, 1-45. https://doi.org/10.1016/B978-0-12-385904-4.00010-X
Ke X.S., Yang B.Y., Cheng X., Chan S.L.F., Zhang J.L. Chem. Eur. J. 2014, 20, 4324-4333. https://doi.org/10.1002/chem.201303972
Bulach V., Sguerra F., Hosseini M.W. Coord. Chem. Rev. 2012, 256, 1468-1478. https://doi.org/10.1016/j.ccr.2012.02.027
Hu J.Y., Ning Y., Meng Y.S., Zhang J., Wu Z.Y., Gao S., Zhang J.L. Chem. Sci. 2017, 8, 2702-2709. https://doi.org/10.1039/C6SC05021B
Sekhosana K.E., Nyokong T. Opt. Mater. (Amst). 2014, 37, 139-146. https://doi.org/10.1016/j.optmat.2014.05.013
Gerasymchuk Y., Tomachynski L., Guzik M., Koll A., Jański J., Guyot Y., Stręk W., Boulon G., Legendziewicz J. J. Photochem. Photobiol. A Chem. 2015, 309, 65-71. https://doi.org/10.1016/j.jphotochem.2015.04.022
Erzunov D., Sarvin I., Belikova A., Vashurin A. Molecules 2022, 27, 4050. https://doi.org/10.3390/molecules27134050
Li B.Y., Yao Y.M., Wang Y.R., Zhang Y., Shen Q. Polyhedron 2008, 27, 709-716. https://doi.org/10.1016/j.poly.2007.10.025
Koshelev D.S., Tcelykh L.O., Mustakimov R.E., Medved'ko A.V., Latipov E.V., Pavlov A.A., Goloveshkin A.S., Gontcharenko V.E., Vlasova K.Y., Burlov A.S., Lepnev L.S., Vatsadze S.Z., Utochnikova V.V. J. Lumin. 2023, 263, 120054. https://doi.org/10.1016/j.jlumin.2023.120054
Kornikov A.I., Mustakimov R.E., Goloveshkin A.S., Tcelykh L.O., Vashchenko A.A., Medvedko A.V., Lepnev L.S., Utochnikova V.V. Org. Electron. 2022, 105, 106492. https://doi.org/10.1016/j.orgel.2022.106492
Han F., Teng Q., Zhang Y., Wang Y., Shen Q. Inorg. Chem. 2011, 50, 2634-2643. https://doi.org/10.1021/ic102529d
Utochnikova V.V., Kalyakina A.S., Bushmarinov I.S., Vashchenko A.A., Marciniak L., Kaczmarek A.M., Van Deun R., Bräse S., Kuzmina N.P. J. Mater. Chem. C 2016, 4, 9848-9855. https://doi.org/10.1039/C6TC03586H
Faulkner S., Pope S.J.A., Burton-Pye B.P. Appl. Spectrosc. Rev. 2005, 40, 1-31. https://doi.org/10.1081/ASR-200038308
Kornilov A.D., Grigoriev M.S., Savinkina E.V. Fine Chemical Technologies 2022, 17, 172-181. https://doi.org/10.32362/2410-6593-2022-17-2-172-181
Li Z.-Y., Shi Y.-L., Liang G.-X., Yang J., Zhuang S.-K., Lin J.-B., Ghodbane A., Tam M.-S., Liang Z.-J., Zha Z.-G., Zhang H.-T. ACS Omega 2020, 5, 15911-15921.
https://doi.org/10.1021/acsomega.0c01054
Numasawa K., Hanaoka K., Saito N., Yamaguchi Y., Ikeno T., Echizen H., Yasunaga M., Komatsu T., Ueno T., Miura M., Nagano T., Urano Y. Angew. Chem. Int. Ed. 2020, 59, 6015-6020. https://doi.org/10.1002/anie.201914826
Pourmadadi M., Mahdi Eshaghi M., Ostovar S., Mohammadi Z., Sharma R.K., Paiva-Santos A.C., Rahmani E., Rahdar A., Pandey S. J. Drug Deliv. Sci. Technol. 2023, 82, 104357. https://doi.org/10.1016/j.jddst.2023.104357
Tazawa H., Shigeyasu K., Noma K., Kagawa S., Sakurai F., Mizuguchi H., Kobayashi H., Imamura T., Fujiwara T. Cancer Sci. 2022, 113, 1919-1929. https://doi.org/10.1111/cas.15369
Hoffman R.M. Lab. Investig. 2015, 95, 432-452. https://doi.org/10.1038/labinvest.2014.154
Dammes N., Peer D. Theranostics 2020, 10, 938-955. https://doi.org/10.7150/thno.37443
Nikfarjam Z., Zargari F., Nowroozi A., Bavi O. Biophys. Rev. 2022, 14, 303-315. https://doi.org/10.1007/s12551-021-00919-1
Celli J.P., Spring B.Q., Rizvi I., Evans C.L., Samkoe K.S., Verma S., Pogue B.W., Hasan T. Chem. Rev. 2010, 110, 2795-2838. https://doi.org/10.1021/cr900300p
Akopov A., Rusanov A., Gerasin A., Kazakov N., Urtenova M., Chistyakov I. Photodiagn. Photodyn. Ther. 2014, 11, 259-264. https://doi.org/10.1016/j.pdpdt.2014.03.011
Suvorov N., Pogorilyy V., Diachkova E., Vasil'ev Y., Mironov A., Grin M. Int. J. Mol. Sci. 2021, 22, 6392. https://doi.org/10.3390/ijms22126392
Grin M.A., Suvorov N.V., Mironov A.F. Mendeleev Commun. 2020, 30, 406-418. https://doi.org/10.1016/j.mencom.2020.07.003
Gouterman M. J. Mol. Spectrosc. 1961, 6, 138-163. https://doi.org/10.1016/0022-2852(61)90236-3
Rabinowitch E. Rev. Mod. Phys. 1944, 16, 226. https://doi.org/10.1103/RevModPhys.16.226
Aita K., Temma T., Kuge Y., Seki K.I., Saji H. Luminescence 2010, 25, 19-24. https://doi.org/10.1002/bio.1136
Faulkner S., Pope S.J.A. J. Am. Chem. Soc. 2003, 125, 10526-10527. https://doi.org/10.1021/ja035634v
Zhao X., Zhuo R., Lu Z., Liu W. Polyhedron 1997, 16, 2755-2759. https://doi.org/10.1016/S0277-5387(97)00029-6
Janicki R., Starynowicz P., Mondry A. Eur. J. Inorg. Chem. 2008, 2008, 3075-3082. https://doi.org/10.1002/ejic.200800249
Jinadasa R.G.W., Hu X., Vicente M.G.H., Smith K.M. J. Med. Chem. 2011, 54, 7464-7476. https://doi.org/10.1021/jm2005139
Parker D., Suturina E.A., Kuprov I., Chilton N.F. Acc. Chem. Res. 2020, 53, 1520-1534. https://doi.org/10.1021/acs.accounts.0c00275
Forsberg J.H. Chapter 153 NMR studies of paramagnetic lanthanide complexes and shift reagents. In: Handbook on the Physics and Chemistry of Rare Earths (Gschneidner K.A., Jr., Eyring LR., Eds.), 1996, 23, pp. 1-68. https://doi.org/10.1016/S0168-1273(96)23004-1