Макроциклические фенантролин-диамиды: Синтез, структура и квантово-химическое моделирование связывания анионов
Аннотация
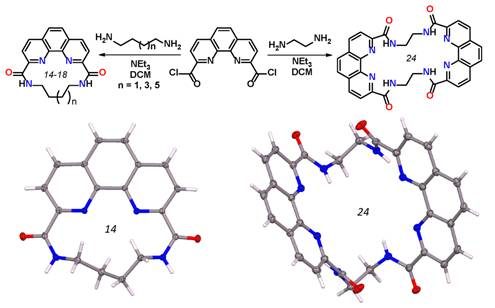
Синтезирован ряд новых макроциклических 1,10-фенантролин-2,9-диамидов, отличающихся размером макроциклической полости (от 14-ти до 24х), а также количеством фенантролиндиамидных фрагментов, входящих в строение макроциклических молекул. Строение всех полученных соединений подтверждено совокупностью спектральных методов анализа, включая спектроскопию ЯМР, ИК-спектроскопию и масс-спектрометрию. Структура двух макроциклов однозначно подтверждена методом рентгеноструктурного анализа. С применением квантово-химических расчетов проведена оптимизация геометрии структур полученных макроциклов и их комплексов с анионами различной природы и геометрии. Для моделирования комплексообразования полученных макроциклов с F- и HF2- проведены дополнительные расчеты с учетом гидратации этих анионов. Расчеты показывают, что 24-членный макроцикл 5 принципиально способен выступать в качестве рецептора F- и HF2- анионов в органических и в водных средах.
Литература
Bencini A., Lippolis V. Coord. Chem. Rev. 2010, 254, 2096–2180. https://doi.org/10.1016/j.ccr.2010.04.008
Alreja P., Kaur N. RSC Adv. 2016, 6, 23169–23217. https://doi.org/10.1039/C6RA00150E
Aragoni M.C., Arca M., Bencini A., Biagini S., Blake A.J., Caltagirone C., Demartin F., De Filippo G., Devillanova F.A., Garau A., Gloe K., Isaia F., Lippolis V., Valtancoli B., Wenzel M. Inorg. Chem. 2008, 47, 8391–8404. https://doi.org/10.1021/ic800548p
Bazzicalupi C., Bencini A., Biagini S., Bianchi A., Faggi E., Giorgi C., Marchetta M., Totti F., Valtancoli B. Chem. Eur. J. 2009, 15, 8049–8063. https://doi.org/10.1002/chem.200900283
Casula A., Nairi V., Fernández-Moreira V., Laguna A., Lippolis V., Garau A., Gimeno M.C. Dalton Trans. 2015, 44, 18506–18517. https://doi.org/10.1039/C5DT02723C
Ishida M., Naruta Y., Tani F. Angew. Chem. Int. Ed. 2010, 49, 91–94. https://doi.org/10.1002/anie.200904859
Kalyakin S.N., Mulagaleeva M.A., Kuzmin V.I., Kuzmina A.A. ChemChemTech [Izv. Vyssh. Uchebn. Zaved. Khim. Khim. Tekhnol.] 2023, 66(1), 56-64. https://doi.org/10.6060/ivkkt.20236601.6674
Gutorova S.V., Logunov M.V., Voroshilov Yu.A., Babain V.A., Shadrin A.Yu., Podoynitsyn S.V., Kharitonov O.V., Firsova L.A., Kozlitin E.A., Ustynyuk Yu.A., Lemport P.S., Nenajdenko V.G., Voronina A.V., Volkovich V.A., Polovov I.B., Dvoeglazov K.N., Mochalov Yu.S., Vidanov V.L., Kascheev V.A., Zaikov Yu.P., Kovrov V.A., Holkina A.S., Suntsov D.Yu., Filimonova E.D., Shmidt O.V., Volk V.I., Melentev A.B., Korchenkin K.K., German K.E., Pokhitonov Yu.A., Tananaev I.G., Pavlyukevich E.Yu., Bagautdinova O.A., Alekseenko V.N., Podrezova L.N., Milyutin V.V., Nekrasova N.A., Kaptakov V.O., Tkachenko L.I., Kalmykov S.N. Russ. J. Gen. Chem. 2024, 94, 243–430. https://doi.org/10.1134/S1070363224150015
Koifman O.I., Ageeva T.A., Beletskaya I.P., Averin A.D., Yakushev A.A., Tomilova L.G., Dubinina T.V., Tsivadze A.Yu., Gorbunova Yu.G., Martynov A.G., Konarev D.V., Khasanov S.S., Lyubovskaya R.N., Lomova T.N., Korolev V.V., Zenkevich E.I., Blaudeck T., von Borczyskowski Ch., Zahn D.R.T., Mironov A.F., Bragina N.A., Ezhov A.V., Zhdanova K.A., Stuzhin P.A., Pakhomov G.L., Rusakova N.V., Semenishyn N.N., Smola S.S., Parfenyuk V.I., Vashurin A.S., Makarov S.V., Dereven’kov I.A., Mamardashvili N.Zh., Kurtikyan T.S., Martirosyan G.G., Burmistrov V.А., Aleksandriiskii V.V., Novikov I.V., Pritmov D.A., Grin M.A., Suvorov N.V., Tsigankov A.A., Fedorov A.Yu., Kuzmina N.S., Nyuchev A.V., Otvagin V.F., Kustov A.V., Belykh D.V., Berezin D.B., Solovieva A.B., Timashev P.S., Milaeva E.R., Gracheva Yu.A., Dodokhova M.A., Safronenko A.V., Shpakovsky D.B., Syrbu S.A., Gubarev Yu.A., Kiselev A.N., Koifman M.O., Lebedeva N.Sh., Yurina E.S. Macroheterocycles 2020, 13, 311–467. https://doi.org/10.6060/mhc200814k
Zhdanova K., Vyal’ba F., Bragina N. Macroheterocycles 2024, 17, 150–179. https://doi.org/10.6060/mhc245875z
Chandler C.J., Deady L.W., Reiss J.A., Tzimos V. J. Heterocyclic Chem. 1982, 19(5), 1017–1019. https://doi.org/10.1002/jhet.5570190507
Chandler C.J., Deady L.W., Reiss J.A. J. Heterocyclic Chem. 1986, 23(5), 1327–1330. https://doi.org/10.1002/jhet.5570230511
Figueiredo J., Carreira-Barral I., Quesada R., Mergny J.-L., Cruz C. Bioorg. Med. Chem. 2022, 73, 116971. https://doi.org/10.1016/j.bmc.2022.116971
Smith D.J., Blake A.J., Wilson C., Champness N.R. Dalton Trans. 2011, 40, 12257. https://doi.org/10.1039/c1dt10815h
Colombo F., Annunziata R., Raimondi L., Benaglia M. Chirality 2006, 18, 446–456. https://doi.org/10.1002/chir.20283
Lemport P.S., Petrov V.S., Matveev P.I., Leksina U.M., Roznyatovsky V.A., Gloriozov I.P., Yatsenko A.V., Tafeenko V.A., Dorovatovskii P.V., Khrustalev V.N., Budylin G.S., Shirshin E.A., Markov V.Yu., Goryunkov A.A., Petrov V.G., Ustynyuk Yu.A., Nenajdenko V.G. Int. J. Mol. Sci. 2023, 24, 10261. https://doi.org/10.3390/ijms241210261
Ustynyuk Yu.A., Petrov V.S., Lemport P.S., Roznyatovsky V.A., Nenajdenko V.G. Russ. J. Org. Chem. 2023, 59, 1709–1713. https://doi.org/10.1134/S1070428023100056
Syrbu S., Ivanova Y., Pukhovskaya S., Kiselev A., Plotnikova A., Torshinina N. Macroheterocycles 2024, 17, 300–305. https://doi.org/10.6060/mhc245796s
Manna U., Das G., Hossain A. Coord. Chem. Rev. 2022, 454, 214357. https://doi.org/10.1016/j.ccr.2021.214357
Zhou Y., Zhang J.F., Yoon J. Chem. Rev. 2014, 114, 5511−5571. https://doi.org/10.1021/cr400352m
Zhan C.-G., Dixon D.A. J. Phys. Chem. A 2004, 108, 2020−2029. https://doi.org/10.1021/jp0311512
Kang J., Sohn D.H., Kim N., Jang S. New J. Chem. 2019, 43, 13690–13695. https://doi.org/10.1039/C9NJ01436E
Xiong S., Kishore M.V.N., Zhou W., He Q. Coord. Chem. Rev. 2022, 461, 214480. https://doi.org/10.1016/j.ccr.2022.214480
Mohammed F.A., Xiao T., Wang L., Elmes R.B.P. Chem. Commun. 2024, 60, 11812–11836. https://doi.org/10.1039/D4CC04521A
Bruker, SAINT, Bruker AXS Inc., Madison, WI, 2013.
Krause L., Herbst-Irmer R., Sheldrick G.M., Stalke D. J. Appl. Cryst. 2015, 48, 3–10. https://doi.org/10.1107/S1600576714022985
Rigaku Oxford Diffraction, CrysAlisPro, Version 1.171. 41.117a; Rigaku Oxford Diffraction: Oxford, UK, 2021.
Sheldrick G.M. Acta Crystallogr. 2015, C71, 3–8. https://doi.org/10.1107/S2053229614024218
Pracht P., Bohle F., Grimme S. Phys. Chem. Chem. Phys. 2020, 22, 7169–7192. https://doi.org/10.1039/C9CP06869D
Laikov D.N., Ustynyuk Yu.A. Russ. Chem. Bull. 2005, 54, 820–826. https://doi.org/10.1007/s11172-005-0329-x
Laikov D.N. J. Chem. Phys. 2020, 153, 114121. https://doi.org/10.1063/5.0014639
Neese F. WIREs Comput. Mol. Sci. 2012, 2, 73–78. https://doi.org/10.1002/wcms.81
Grimme S., Ehrlich S., Goerigk L. J. Comput. Chem. 2011, 32, 1456–1465. https://doi.org/10.1002/jcc.21759